Différence entre le benzaldéhyde et la benzophénone
Le différence clé entre le benzaldéhyde et la benzophénone Le benzaldéhyde est un aldéhyde, tandis que la benzophénone est une cétone.
La benzaldéhyde et la benzophénone sont des composés carbonyle aromatiques. Cependant, le benzaldéhyde a un groupe phényle attaché au groupe carbonyle parce que l'autre côté de ce carbone carbonyle a un atome d'hydrogène car il s'agit d'un aldéhyde. Mais, en benzophénone, les deux côtés du carbone carbonyle ont des groupes phényle.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le benzaldéhyde
3. Qu'est-ce que la benzophénone
4. Comparaison côte à côte - benzaldéhyde vs benzophénone sous forme tabulaire
5. Résumé
Qu'est-ce que le benzaldéhyde?
Le benzaldéhyde est un aldéhyde aromatique ayant la formule chimique C6H5Chou. Il a un groupe phényle attaché à un groupe fonctionnel aldéhyde. De plus, c'est l'aldéhyde aromatique le plus simple. Il se produit comme un liquide incolore et a une odeur caractéristique semblable à des amandes. De plus, sa masse molaire est de 106.12 g / mol. Et, son point de fusion est -57.12 ° C tandis que le point d'ébullition est de 178.1 ° C.
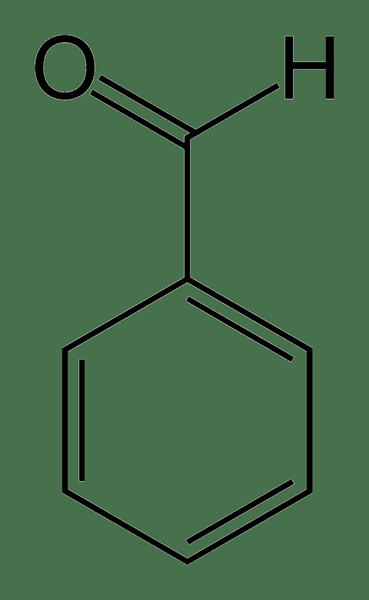
Figure 01: Structure du benzaldéhyde
Concernant la production de benzaldéhyde, les principales voies de la production de ce composé sont la chloration et l'oxydation de la phase liquide du toluène. Cependant, ce composé se produit également naturellement dans de nombreux aliments; Par exemple, dans les amandes. Par conséquent, l'une des principales utilisations de ce composé est son utilisation comme une saveur d'amande dans les aliments et les produits parfumés.
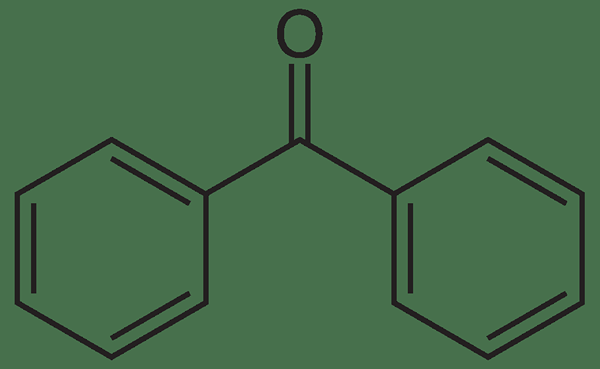
Qu'est-ce que la benzophénone?
La benzophénone est une cétone aromatique ayant la formule chimique C13H10O. Il s'agit d'une cétone aromatique et a deux anneaux de benzène attachés au même atome de carbone du groupe carbonyle. Nous pouvons l'abréger comme PH2O où le pH fait référence au «phénol» (un autre nom pour la bague benzène).

Figure 02: Structure de la benzophénone
En regardant les propriétés de la benzophénone, sa masse molaire est de 182.22 g / mol. Il a une odeur de type géranium, et il se produit comme un solide blanc à la température et à la pression standard. De plus, ce composé est insoluble dans l'eau mais, soluble dans certains solvants organiques. Le point de fusion est 48.5 ° C tandis que le point d'ébullition est 305.4 ° C. En outre, nous pouvons produire ce composé via l'oxydation catalysée par le cuivre de diphénylméthane avec l'air.
Lorsque vous envisagez les utilisations de la benzophénone, il est utile comme élément constitutif pour la synthèse de nombreux composés organiques, comme photo-initiateur dans les applications de durcissement UV, comme bloqueur UV pour les packages en plastique, etc.
Quelle est la différence entre le benzaldéhyde et la benzophénone?
Le benzaldéhyde est un aldéhyde aromatique ayant la formule chimique C6H5Cho tandis que la benzophénone est une cétone aromatique ayant la formule chimique C13HdixO. Ainsi, la principale différence entre le benzaldéhyde et la benzophénone est que le benzaldéhyde est un aldéhyde, tandis que la benzophénone est une cétone. De plus, le benzaldéhyde a une odeur caractéristique de type amande, mais la benzophénone a une odeur de type géranium.
De plus, si l'on considère les structures chimiques de ces composés, la différence entre le benzaldéhyde et la benzophénone est que le benzaldéhyde a un groupe phényle attaché à un groupe fonctionnel aldéhyde, tandis que la benzophénone a deux groupes phényle attachés aux deux côtés du carbone carbonyle carbone.
L'infographie ci-dessous montre plus de comparaisons concernant la différence entre le benzaldéhyde et la benzophénone.
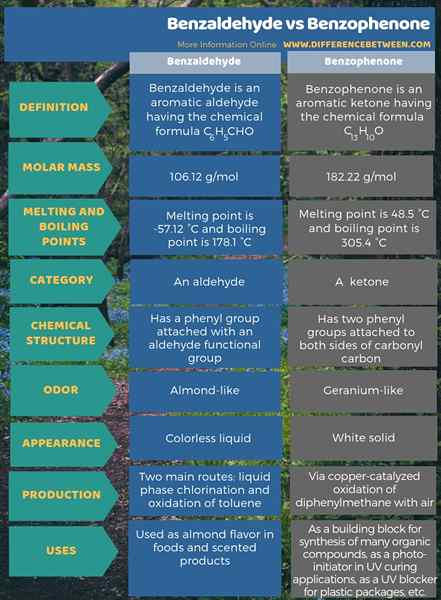
Résumé - Benzaldéhyde vs benzophénone
Le benzaldéhyde est un aldéhyde aromatique ayant la formule chimique C6H5Cho tandis que la benzophénone est une cétone aromatique ayant la formule chimique C13HdixO. En résumé, la principale différence entre le benzaldéhyde et la benzophénone est que le benzaldéhyde est un aldéhyde, tandis que la benzophénone est une cétone.
Référence:
1. «Benzaldéhyde.»Wikipedia, Wikimedia Foundation, 15 juin 2019, disponible ici.
Image gracieuseté:
1. «Benzaldéhyde» par NeuroKer - Propre travaux (domaine public) via Commons Wikimedia
2. «Benzophénon» par Wikimuzg - Propre travaux (CC BY-SA 3.0) via Commons Wikimedia


