Différence entre le sulfate de baryum et le sulfure de baryum

Le différence clé entre le sulfate de baryum et le sulfure de baryum est que Le sulfate de baryum est un composé non toxique tandis que le sulfure de baryum est un composé hautement toxique.
Le sulfate de baryum et le sulfure de baryum sont des composés inorganiques. Ce sont des sels d'élément chimique de baryum. Nous pouvons facilement obtenir du sulfate de baryum à partir de sulfure de baryum.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le sulfate de baryum
3. Qu'est-ce que le sulfure de baryum
4. Relation entre sulfate et sulfure de baryum
5. Comparaison côte à côte - sulfate vs sulfure de baryum sous forme tabulaire
6. Résumé
Qu'est-ce que le sulfate de baryum?
Le sulfate de baryum est un composé inorganique ayant la formule chimique Baso4. Il s'agit d'un composé solide à température ambiante et à la pression et apparaît comme une substance solide cristalline blanche qui est inodore et insoluble dans l'eau. Ce composé se produit naturellement dans le dépôt minéral «baryte». Ce minéral est la principale source commerciale de baryum et de ses composés. Le sulfate de baryum a une forte densité et est également insoluble dans l'alcool. Cependant, nous pouvons dissoudre cette substance dans l'acide sulfurique chaud et concentré.

Figure 01: sulfate de baryum
Il existe de nombreuses utilisations différentes du sulfate de baryum, y compris son utilisation comme composante du liquide de forage du puits d'huile où il peut augmenter la densité du fluide, l'utilisation médicale comme agent radiocontraste pour les processus d'imagerie aux rayons X, comme composant du pigment blanc pour les peintures , un revêtement sur le papier photographique pour augmenter la réflectivité de l'image, un remplissage pour les plastiques, utile dans les tests de sol, etc.
La plupart du sulfate de baryum disponible dans le commerce est obtenu industriellement à partir de dépôts minéraux de baryte. Souvent, ce minéral est très impur. Par conséquent, nous devons le traiter par une réduction carbothermique afin d'obtenir du sulfure de baryum. À partir du sulfure de baryum, nous pouvons facilement obtenir du sulfate de baryum très pur.
Les sels solubles de sel de baryum sont considérés comme des composés modérément toxiques. Mais en raison de la nature très insoluble de ce composé, le sulfate de baryum est considéré comme un composé non toxique.
Qu'est-ce que le sulfure de baryum?
Le sulfure de baryum est un composé inorganique ayant la formule chimique BAS. C'est un composé solide incolore, mais il peut également y avoir des variations colorées en raison de la présence d'impuretés. Ce composé est relativement soluble dans l'eau et se transforme facilement en forme d'oxyde (oxyde de baryum), forme de carbonate et halogénures. Cependant, c'est insoluble dans les alcools. Le sulfure de baryum est important comme précurseur de la production d'autres composés de baryum tels que le carbonate de baryum, le pigment lithopone, etc.
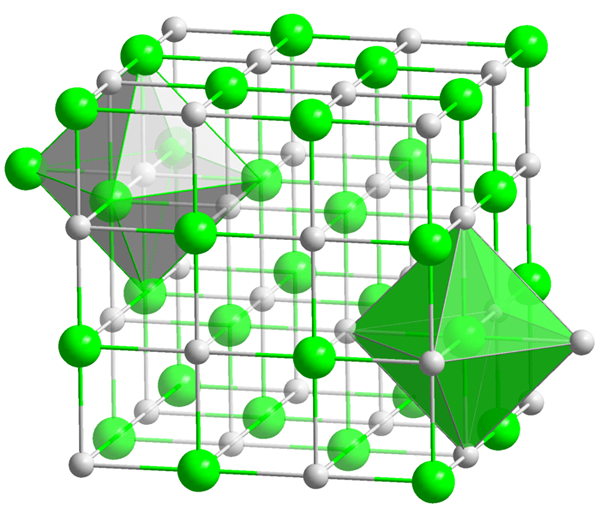
Figure 02: Structure cristalline du sulfure de baryum
Actuellement, le sulfure de baryum est produit grâce à un processus amélioré de processus de Casciarole, qui utilise Coke. Cela implique une réaction carbothermique. Ici, le sulfure de baryum cristallise dans la structure NaCl, montrant les centres octaédriques de baryum et de sulfure.
Plus important encore, le sulfure de baryum est toxique. Il peut évoluer facilement en sulfure d'hydrogène au contact de l'eau. Le sulfure d'hydrogène est un gaz toxique. La plupart des sulfures apparentés, tels que le sulfure de calcium (CAS), ont cette capacité.
Quelle est la relation entre le sulfate de baryum et le sulfure de baryum?
- Le sulfate de baryum et le sulfure de baryum sont des composés inorganiques.
- Ce sont des sels d'élément chimique de baryum.
- Nous pouvons facilement obtenir du sulfate de baryum à partir de sulfure de baryum.
Quelle est la différence entre le sulfate de baryum et le sulfure de baryum?
Le sulfate de baryum et le sulfure de baryum sont des composés inorganiques. La principale différence entre le sulfate de baryum et le sulfure de baryum est que le sulfate de baryum est un composé non toxique tandis que le sulfure de baryum est un composé hautement toxique. Nous pouvons facilement obtenir du sulfate de baryum à partir de sulfure de baryum.
Ci-dessous énumère les différences entre le sulfate de baryum et le sulfure de baryum sous forme tabulaire.
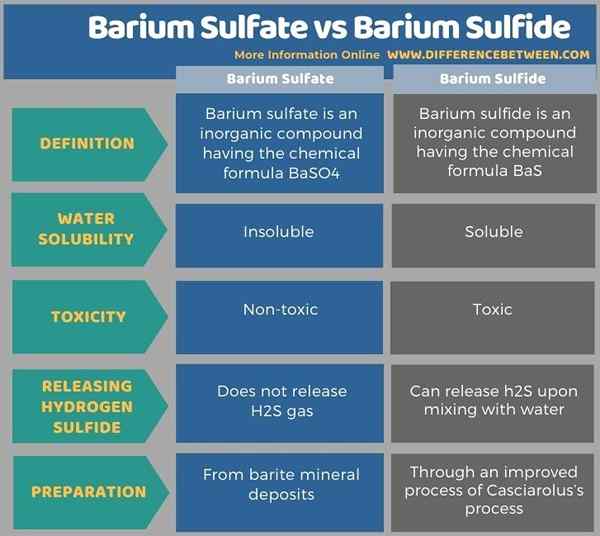
Résumé - Sulfate de baryum vs sulfure de baryum
Le sulfate de baryum et le sulfure de baryum sont des composés inorganiques. La principale différence entre le sulfate de baryum et le sulfure de baryum est que le sulfate de baryum est un composé non toxique tandis que le sulfure de baryum est un composé hautement toxique.
Référence:
1. «Aperçu du sulfure de baryum.”Science Direct, disponible ici.
Image gracieuseté:
1. «Bariumsulfatpulver» par de: Benutzer: The-Viewer - DE.Wikipedia (CC BY-SA 3.0) via Commons Wikimedia
2. «NaCl Polyhedra» par Solid State - Propre travaux (domaine public) via Commons Wikimedia


