Différence entre les allotropes et les isotopes
Le différence clé entre les allotropes et les isotopes Les allotropes sont pris en compte au niveau moléculaire tandis que les isotopes sont considérés au niveau atomique.
Il y a environ 118 éléments dans le tableau périodique selon leur numéro atomique. Un élément est une substance chimique qui ne se compose qu'un seul type d'atomes; Par conséquent, ils sont purs. Les allotropes sont des formes différentes du même composé tandis que les isotopes sont des formes différentes du même élément.
CONTENU
1. Aperçu et différence clé
2. Que sont les allotropes
3. Que sont les isotopes
4. Comparaison côte à côte - Allotropes vs isotopes sous forme tabulaire
5. Résumé
Que sont les allotropes?
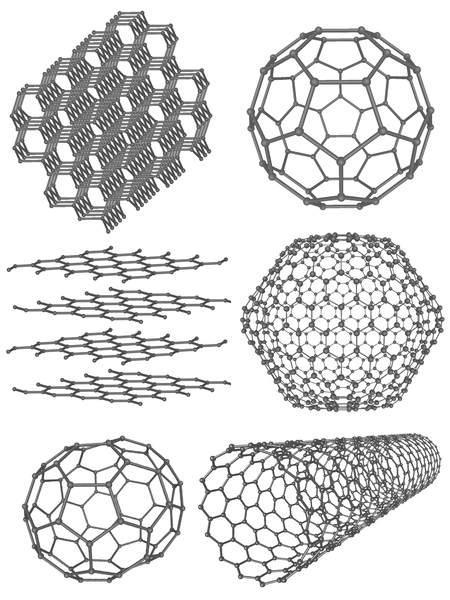
Les allotropes sont des formes différentes du même élément au niveau moléculaire. Ils montrent différentes propriétés physiques. Parmi tous les éléments chimiques, le carbone, l'oxygène, le soufre et le phosphore sont les principaux éléments qui ont des allotropes. Le carbone a un grand nombre d'allotropes. Les huit allotropes de carbone diffèrent en grande partie les uns des autres. Par exemple, le diamant est l'allotrope le plus fort du carbone alors que le graphite est moins fort. Les nanotubes de carbone, le fullerène et le carbone amorphe sont quelques autres allotropes de carbone.

Figure 1: Allotropes de carbone
Pour l'élément oxygène, il y a deux allotropes courants comme O2 et O3. O2 est abondant que O3. Normalement, dans la nature, certains allotropes sont plus abondants que d'autres en raison de leur stabilité. Le phosphore a trois allotropes en tant que phosphore rouge, blanc et noir. À partir de ceux-ci, le phosphore rouge et blanc est le plus courant. Les allotropes diffèrent les uns des autres en raison de la disposition atomique, du nombre d'atomes, etc.
Que sont les isotopes?
Les isotopes sont différentes formes d'atomes du même élément chimique. Ils sont différents les uns des autres car ils ont un nombre différent de neutrons. Étant donné que le nombre de neutrons est différent, leur nombre de masse diffère également.
Cependant, les isotopes du même élément ont le même nombre de protons et de neutrons. Différents isotopes sont présents en quantités variables, et nous pouvons donner cela en pourcentage de la valeur appelée abondance relative. Par exemple, l'hydrogène a trois isotopes comme protium, deutérium et tritium. Leur nombre de neutrons et d'abondances relatives sont les suivants.

Figure 2: Différentes isotopes de l'élément chimique Hydrogène
Le nombre de neutrons qu'un noyau peut tenir diffère d'un élément à l'autre. Parmi ces isotopes, seuls certains sont stables. Par exemple, l'oxygène a trois isotopes stables, et Tin a dix isotopes stables. La plupart du temps, les éléments simples ont le même numéro de neutrons que le numéro de proton. Mais, dans des éléments lourds, il y a plus de neutrons que de protons. Le nombre de neutrons est important pour équilibrer la stabilité des noyaux. Lorsque les noyaux sont trop lourds, ils deviennent instables; Par conséquent, ces isotopes deviennent radioactifs. Par exemple, 238U émet un rayonnement et se désintègre à des noyaux beaucoup plus petits. Les isotopes peuvent avoir des propriétés différentes en raison de leurs différentes masses. Par exemple, ils peuvent avoir des tours différents; ainsi leurs spectres RMN diffèrent. Cependant, leur nombre d'électrons est similaire, donnant lieu à un comportement chimique similaire.
Quelle est la différence entre les allotropes et les isotopes?
Les allotropes sont des formes différentes du même élément au niveau moléculaire. Les isotopes sont différentes formes d'atomes du même élément chimique. La principale différence entre les allotropes et les isotopes est que les allotropes sont considérés au niveau moléculaire, tandis que les isotopes sont considérés au niveau atomique. De plus, une autre différence entre les allotropes et les isotopes est que les allotropes diffèrent les uns des autres sur le chemin que les atomes sont organisés tandis que les isotopes diffèrent les uns des autres dans le nombre de neutrons.
L'infographie ci-dessous montre plus de détails sur la différence entre les allotropes et les isotopes.

Résumé - Allotropes vs isotopes
Bien que les termes allotrope et isotope semblent similaires, ils sont très distincts les uns des autres en fonction de leur signification. La principale différence entre les allotropes et les isotopes est que les allotropes sont considérés au niveau moléculaire, tandis que les isotopes sont considérés au niveau atomique.
Référence:
1. Helmenstine, Anne Marie, «Définition d'allotrope et exemples."Thoughtco, Jan. 13, 2019, disponible ici.
2. Helmenstine, Anne Marie, «Définition des isotopes et exemples en chimie.”Thoughtco, oct. 22, 2018, disponible ici.
Image gracieuseté:
1. «Allotropes de carbone» par mstroeck (talk) (uploads) - propre travail (cc by-sa 3.0) via Commons Wikimedia


