Quelle est la différence entre l'acide carbonique et le bicarbonate
Le différence clé entre l'acide carbonique et le bicarbonate est que l'acide carbonique est un composé chimique neutre, tandis que le bicarbonate est un composé chimique chargé négativement.
L'acide carbonique est un acide faible qui se forme en solution lorsque le dioxyde de carbone se dissout dans l'eau, avec la formule chimique H2CO3. Le bicarbonate se forme par la combinaison de trois atomes d'oxygène, un atome d'hydrogène et un atome de carbone avec la formule chimique HCO3-.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que l'acide carbonique
3. Qu'est-ce que le bicarbonate
4. Acide carbonique vs bicarbonate sous forme tabulaire
5. Résumé - Acide carbonique vs bicarbonate
Qu'est-ce que l'acide carbonique?
L'acide carbonique est H2CO3. Parfois, nous donnons ce nom aux solutions ayant un dioxyde de carbone dissous dans l'eau ou l'eau gazeuse. En effet, l'eau gazeuse contient une petite quantité de H2CO3. De plus, l'acide carbonique est un acide faible, et il peut former deux types de sels en tant que carbonates et bicarbonates. La masse molaire de ce composé est 62.024 g / mol.
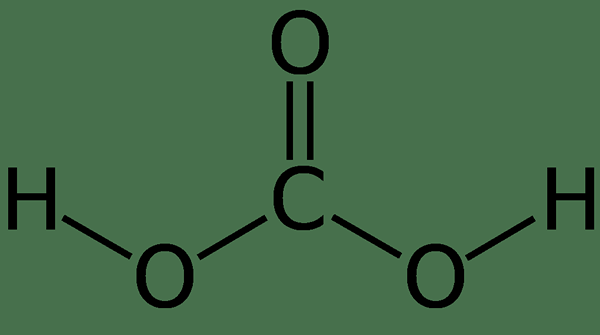
Figure 01: La structure chimique de l'acide carbonique
Lorsque le dioxyde de carbone se dissout dans l'eau, il entre un équilibre entre le dioxyde de carbone et l'acide carbonique. L'équilibre est le suivant:
CO2 + H2O ⟷ H2CO3
Si nous ajoutons un excès d'acide carbonique à une base, il donne du bicarbonate. Mais, s'il y a un excès de base, alors l'acide carbonique a tendance à donner des sels gazeux. Plus précisément, l'acide carbonique est un composé d'acide carboxylique qui a deux substituants de groupe hydroxyle attachées au carbone carbonyle. De plus, c'est un acide polyprotique, qui est capable de donner des protons. Il a deux protons amovibles, il est donc spécifiquement diprotique.
Qu'est-ce que le bicarbonate?
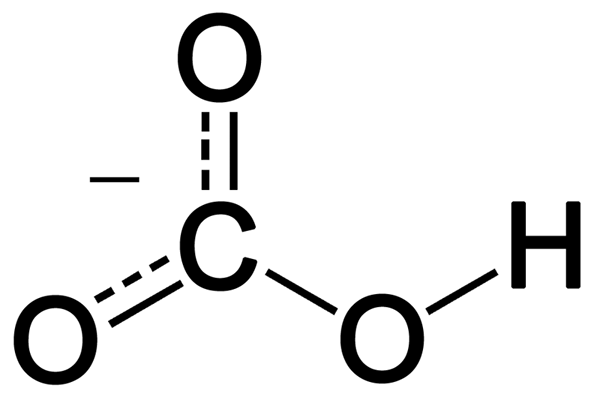
Le bicarbonate se forme par la combinaison de trois atomes d'oxygène, un atome d'hydrogène et un atome de carbone. Le produit de cette combinaison peut être un ion ou un composé avec plus d'électrons que de protons. Nous pouvons le décrire comme une espèce chimique ayant la formule chimique HCO3-.

Figure 02: La structure chimique de l'anion bicarbonate
Ce composé est une partie cruciale du système de mise en mémoire tampon du pH du corps, en termes simples: il est responsable de garder son sang dans un état qui n'est pas trop acide ou trop basique. De plus, il sert de moyen de garder les jus digestifs en échec une fois l'estomac. De plus, l'acide carbonique dans l'eau de pluie forme des ions bicarbonate lorsqu'il fait des rochers. Ce flux d'ions bicarbonate est important pour maintenir le cycle du carbone.
Quelle est la différence entre l'acide carbonique et le bicarbonate?
L'acide carbonique est un acide faible qui se forme en solution lorsque le dioxyde de carbone se dissout dans l'eau, et sa formule chimique est H2CO3. Le bicarbonate se forme par la combinaison de trois atomes d'oxygène, un atome d'hydrogène et un atome de carbone avec la formule chimique HCO3-. La principale différence entre l'acide carbonique et le bicarbonate est que l'acide carbonique est un composé chimique neutre, tandis que le bicarbonate est un composé chimique chargé négativement. De plus, l'acide carbonique est utilisé pour fabriquer des boissons pétillantes, pétillantes, traiter les dermatitides, le rince-bouche, etc., tandis que le bicarbonate est utilisé dans les préparations alimentaires telles que la cuisson (en tant qu'agent de levain), et elle donne la possibilité de résister aux changements de pH.
L'infographie suivante résume la différence entre l'acide carbonique et le bicarbonate sous forme tabulaire pour une comparaison côte à côte.
Résumé - Acide carbonique vs bicarbonate
L'acide carbonique est H2CO3. Le bicarbonate se forme par la combinaison de trois atomes d'oxygène, un atome d'hydrogène et un atome de carbone, avec la formule chimique HCO3-. La principale différence entre l'acide carbonique et le bicarbonate est que l'acide carbonique est un composé chimique neutre, tandis que le bicarbonate est un composé chimique chargé négativement.
Référence:
1. «Que sont les bicarbonates? - Structure, usages et effets sur la santé des bicarbonates."Byju's, 19 août. 2021.
Image gracieuseté:
1. «Carbonic Acid 2d» par Eetwartti - propre travail basé sur l'image: carbonic-acid-2d.PNG (domaine public) via Commons Wikimedia
2. «Bicarbonate Resonance» par Hellbus - Propre travaux (CC BY-SA 3.0) via Commons Wikimedia


