Différence entre les ions polyatomiques et les composés
Le différence clé entre les ions polyatomiques et les composés est que le Les ions polyatomiques ont une charge électrique positive ou négative alors que les composés n'ont pas de charge électrique nette.
Un ion polyatomique est un terme que nous utilisons pour nommer des espèces chimiques contenant deux atomes ou plus qui ont une charge électrique négative ou positive nette. La charge électrique de cet ion est le résultat du nombre d'électrons présents dans chaque atome; S'il y a plus d'électrons que le nombre total de protons dans les atomes, il obtient une charge négative nette et vice versa. Les composés, en revanche, sont des espèces chimiques sans charge électrique. Ils ont un nombre égal d'électrons et de protons.
CONTENU
1. Aperçu et différence clé
2. Quels sont les ions polyatomiques
3. Que sont les composés
4. Comparaison côte à côte - ions polyatomiques vs composés sous forme tabulaire
5. Résumé
Quels sont les ions polyatomiques?
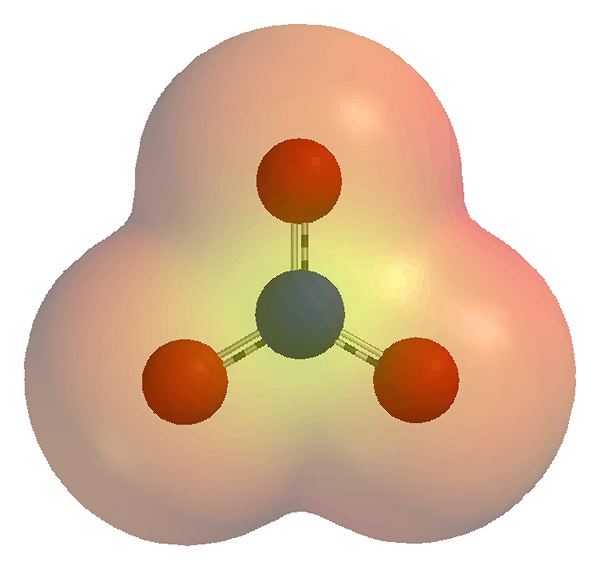
Les ions polyatomiques sont des espèces chimiques ayant deux atomes ou plus et une charge électrique nette. Cette charge électrique peut être soit une charge positive, soit une charge négative en fonction du nombre d'électrons et de protons présents dans les espèces chimiques. Un synonyme de cette espèce est «ion moléculaire». Les atomes se lient les uns avec les autres. Nous pouvons considérer certains complexes métalliques comme des ions polyatomiques s'ils agissent comme une seule unité. En revanche, les ions monoatomiques sont des atomes uniques qui portent une charge électrique. Nous pouvons trouver ces ions dans des composés de sel, des composés de coordination et de nombreux autres composés ioniques; Dans le cadre du composé.

Figure 01: un ion nitrate
Quelques exemples d'ions polyatomiques:
- Ion acétate (ch3ROUCOULER-)
- Ion benzoate (c6H5ROUCOULER-)
- Ion carbonate (CO32-)
- Ion cyanure (CN-)
- Ion hydroxyde (oh-)
- Ion nitrite (non2-)
- Ion ammonium (NH4+)
Que sont les composés?
Les composés sont des espèces chimiques contenant des molécules identiques se composent d'atomes de deux ou plusieurs éléments chimiques. Par conséquent, ces espèces chimiques ne portent pas de charge électrique nette. Par conséquent, ce sont des espèces neutres. Les atomes se lient entre eux via des liaisons covalentes, des liaisons de coordination ou des liaisons ioniques. De plus, s'il y a une molécule contenant deux atomes ou plus du même élément lié les uns aux autres, ce n'est pas un composé car il n'y a pas d'éléments différents.
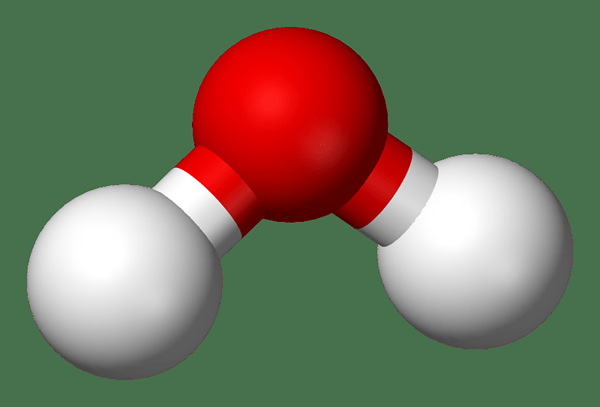
Figure 02: Une molécule d'eau
De plus, selon la définition, il existe 4 types de composés comme suit:
- Molécules ayant des combinaisons de différents éléments chimiques
- Les composés ioniques sont constitués de liaisons ioniques
- Composés intermétalliques ayant des obligations métalliques
- Les complexes de coordination sont constitués de liaisons coordonnées
Nous pouvons utiliser une formule chimique afin d'exprimer les éléments chimiques et le rapport entre eux présent dans un composé. Par exemple, la formule chimique de la molécule d'eau est H2O. Il a deux atomes d'hydrogène et un atome d'oxygène, mais la molécule n'a pas de charge électrique nette; C'est donc un composé chimique.
Quelle est la différence entre les ions polyatomiques et les composés?
Les ions polyatomiques sont des espèces chimiques ayant deux atomes ou plus et une charge électrique nette. Ils ont une charge électrique positive ou négative. Les composés sont des espèces chimiques contenant des molécules identiques se composent d'atomes de deux ou plusieurs éléments chimiques. Ils n'ont pas de charge électrique nette. C'est la principale différence entre les ions polyatomiques et les composés. De plus, les ions polyatomiques ont des liaisons covalentes ou des liaisons de coordination entre les atomes. Tandis que les composés peuvent avoir des liaisons covalentes, des liaisons ioniques, des liaisons métalliques ou des liaisons de coordination entre les atomes.
L'infographie ci-dessous présente la différence entre les ions polyatomiques et les composés sous forme tabulaire.

Résumé - Ions polyatomiques vs composés
La principale différence entre les ions polyatomiques et les composés est que les ions polyatomiques ont une charge électrique positive ou négative tandis que les composés n'ont pas de charge électrique nette. Cela est principalement dû au fait que les ions polyatomiques ont un nombre déséquilibré d'électrons et de protons tandis que les composés ont un nombre égal d'électrons et de protons.
Référence:
1. Helmenstine, Anne Marie, Ph.D. «Définition et exemples de la définition et des exemples de l'ion polyatomique.”Thoughtco, Jun. 22, 2018. Disponible ici
2. Noller, Carl R., et al. "Composé chimique.»Encyclopædia Britannica, Encyclopædia Britannica, Inc., 6 décembre. 2016. Disponible ici
Image gracieuseté:
1.«Nitrate-ion-elpot» par Benjah-Bmm27 - Propre travaux, (domaine public) via Commons Wikimedia
2.«Water-3D-balls» par Benjah-Bmm27 - Propre travaux, (domaine public) via Commons Wikimedia


