Différence entre les liaisons chimiques localisées et délocalisées
Le différence clé entre les liaisons chimiques localisées et délocalisées est Cette liaison chimique localisée est une liaison spécifique ou une paire d'électrons solitaires sur un atome spécifique alors que la liaison chimique délocalisée est une liaison spécifique qui n'est pas associée à un seul atome ou à une liaison covalente.
Une liaison chimique est un lien entre deux atomes. Cette connexion se produit en raison du chevauchement des orbitales moléculaires. Il existe deux formes principales de liaisons comme des liaisons chimiques localisées et délocalisées. Les liaisons chimiques localisées sont les chevauchements orbitaux moléculaires normaux tels que les liaisons Sigma et les liaisons PI. Cependant, les liaisons chimiques délocalisées sont différentes. Ces liaisons se forment lorsque plusieurs liaisons localisées se mélangent entre elles. Plus de détails sont ci-dessous.
CONTENU
1. Aperçu et différence clé
2. Que sont les liaisons chimiques localisées
3. Que sont les liaisons chimiques délocalisées
4. Comparaison côte à côte - liaisons chimiques localisées vs délocales sous forme tabulaire
5. Résumé
Que sont les liaisons chimiques localisées?
Les liaisons chimiques localisées sont des liaisons Sigma et Pi normales ou des paires d'électrons solitaires qui existent sur un seul atome. Ces liaisons sont concentrées sur une région limitée d'une molécule. Ces régions ont une distribution d'électrons concentrée. En d'autres termes, la densité électronique de cette région est très élevée.

Figure 01: une liaison Sigma - une liaison chimique localisée
Une liaison localisée se forme lorsque deux orbitales moléculaires de deux atomes séparés se chevauchent. Les obligations Sigma peuvent se former en raison du chevauchement de deux orbitales S, de deux orbitales P ou du chevauchement S-P.
Que sont les liaisons chimiques délocalisées?
Les liaisons chimiques délocalisées sont les liaisons chimiques qui ne s'associent pas à un seul atome mais à plusieurs atomes ou autres liaisons chimiques. Nous appelons les électrons de ces liaisons comme des «électrons délocalisés». La délocalisation se produit dans le système PI conjugué. Un système PI conjugué a des liaisons doubles et des liaisons simples dans un motif alternatif.
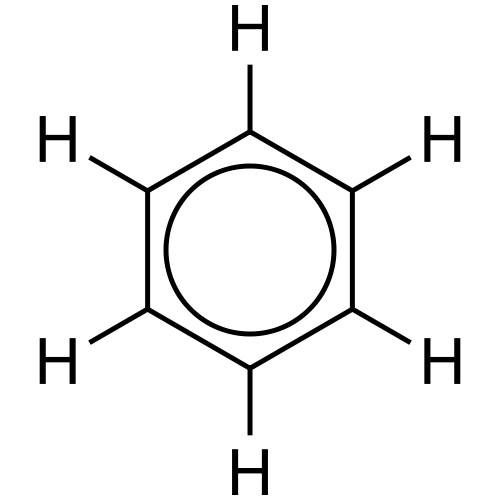
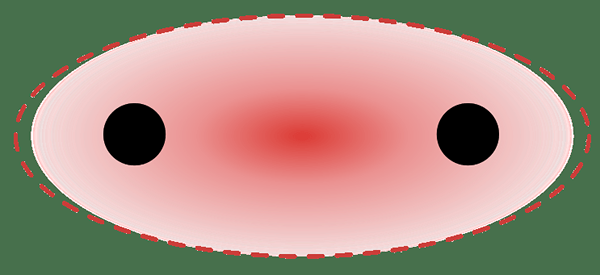
Figure 02: Delocalisation des électrons
Par exemple, l'anneau de benzène a trois liaisons simples et trois doubles liaisons dans un motif alternatif. Chaque atome de carbone de cette bague a une orbitale p qui ne subit pas de chevauchement frontal. Par conséquent, ces orbitales P peuvent se chevaucher latérales. Ce type de chevauchement est la délocalisation. Nous pouvons indiquer cela comme deux cercles sur le dessus de l'anneau de benzène et le bas de l'anneau. Ces électrons sont libres de se déplacer à travers la molécule car ils n'ont pas de liaison permanente à un seul atome ou à une liaison covalente.
Quelle est la différence entre les liaisons chimiques localisées et délocalisées?
Les liaisons chimiques localisées sont des liaisons Sigma et Pi normales ou des paires d'électrons solitaires qui existent sur un seul atome. Ces obligations se forment dues à un chevauchement frontal entre les orbitales S, les orbitales P ou les orbitales S et P. De plus, ces électrons sont limités à une région particulière entre deux atomes distincts. Les liaisons chimiques délocalisées sont les liaisons chimiques qui ne s'associent pas à un seul atome mais à plusieurs atomes ou autres liaisons chimiques. Ces liaisons ont des électrons répartis dans la molécule qui sont libres de se déplacer. Ces obligations se forment en raison du chevauchement latéral des orbitales p. C'est la principale différence entre les liaisons chimiques localisées et délocalisées.
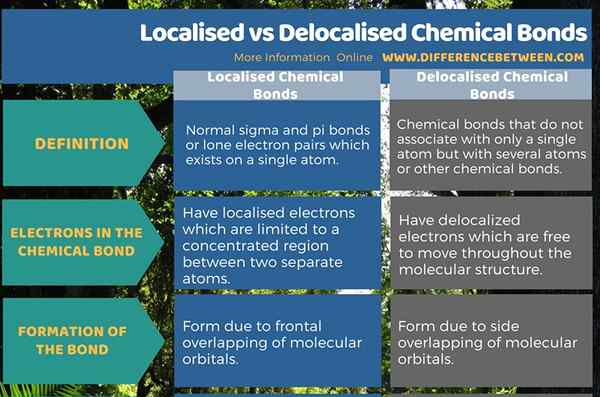
Résumé - Bond chimiques localisés vs délocalisés
Une liaison chimique est un lien entre deux atomes. Il existe deux formes de liaisons chimiques comme des liaisons chimiques localisées et délocalisées. La différence entre les liaisons chimiques localisées et délocalisées est qu'une liaison chimique localisée est une liaison spécifique ou une paire d'électrons solitaires sur un atome spécifique alors qu'une liaison chimique délocalisée est une liaison spécifique qui n'est pas associée à un seul atome ou à une liaison covalente.
Référence:
1. LibreTexts. «Delocalisation des électrons.”Chemistry LibreTexts, LibreTexts, 20 déc. 2016. Disponible ici
2. «Orbitales moléculaires localisées.»Wikipedia, Wikimedia Foundation, 19 juin 2018. Disponible ici
Image gracieuseté:
1.«Sigma Bond'By Svg: Zoofari; Raster: Anselm H. C. Corne (cc by-sa 3.0) via Commons Wikimedia
2.'Benzène-6H-Delocalized' par une élite - propre travail, (CC BY-SA 3.0) via Commons Wikimedia


