Différence entre le point isoélectrique et isoionique
Différence clé - isoélectrique vs isoionique Indiquer
Les deux termes Isoelectric Point et Isoionic Point décrivent le même concept biochimique sur les acides aminés; Le point isoélectrique ou le point isoionique est le pH auquel les charges positives d'un acide aminé équivaut aux charges négatives du même acide aminé. Ainsi, il y a aucune différence entre les termes isoélectriques et point isoionique.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le point isoélectrique ou le point isoionique
3. Isoélectrique vs point isoionique
4. Résumé
Qu'est-ce que le point isoélectrique ou le point isoionique?
Le point isoélectrique ou le point isoionique d'un acide aminé est le pH à laquelle les charges positives d'un acide aminé égal aux charges négatives du même acide aminé. Il est indiqué par pi. Puisqu'il n'y a pas de charge électrique nette dans l'acide aminé, il ne peut pas migrer dans un champ électrique. Par conséquent, le point isoélectrique est le point auquel l'acide aminé est neutre.
Au point isoélectrique, une zwitterion est formée. Une Zwitterion est une molécule dipolaire qui a plus de deux groupes fonctionnels ayant des charges positives et négatives (groupes fonctionnels chargés positivement et groupes fonctionnels chargés négativement). Les charges positives sur les groupes fonctionnels devraient être égales aux charges négatives présentes sur les groupes fonctionnels de l'acide aminé. Cela fait la charge électrique nette du zwitterion zéro.

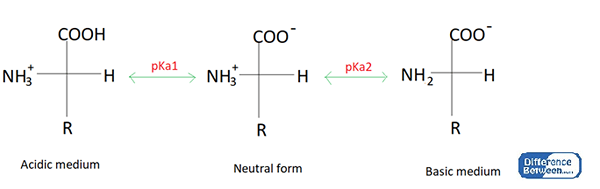
Figure 01: les formes acides, de base et neutres d'un acide aminé
Au point isoïonique, la Zwitterion est la forme dominante de l'acide aminé. La valeur PI peut être obtenue en utilisant les valeurs PKA de la charge positive nette et des formes de charge négative nettes des acides aminés dans des supports acides et basiques.
- S'il n'y a pas de groupes fonctionnels chargés dans la chaîne latérale de l'acide aminé,
pi = ½ (PKA1 + pka2) Où PKA1 et pka2 sont les valeurs PKA de l'acide aminé dans les médiums acides et basiques.
- S'il y a des chaînes latérales acides, Pi est plus faible que prévu.
- S'il y a des chaînes latérales de base, Pi est plus élevé que prévu.
Quelle est la différence entre le point isoélectrique et isoionique?
- Le point isoélectrique, également connu sous le nom de point isoionique, d'un acide aminé est le pH auquel les charges positives d'un acide aminé égal aux charges négatives du même acide aminé, indiqué par pi.
Résumé - Isoélectrique vs isoionique Indiquer
Il n'y a pas de différence entre les termes Isoelectric Point et Isoionic Point. Les deux termes sont utilisés pour nommer le pH auquel il n'y a pas de charge électrique nette dans un acide aminé.
Référence:
1. Hunt, Ian R. «Point isoélectronique, PI." CH27: point isoélectronique. Disponible ici
2. «Point isoionique.»Wikipedia, Wikimedia Foundation, 17 février. 2018. Disponible ici
3. «Zwitterion.»Wikipedia, Wikimedia Foundation, 20 mars. 2018. Disponible ici


