Différence entre le cyanure et le nitrile
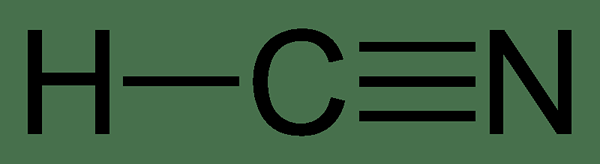
Le différence clé entre le cyanure et le nitrile Le terme cyanure fait référence à tout composé chimique contenant un groupe cyano. Pendant ce temps, le terme nitrile fait référence à tout composé organique contenant un groupe Cyano.
Nous utilisons généralement les termes cyanure et nitrile interchangeables parce que ces deux termes se réfèrent au groupe C≡N ou au groupe Cyano. Mais, ils sont différents les uns des autres parce que le terme nitrile n'est utilisé que pour le composé organique ayant le groupe Cyano tandis que le terme cyanure fait référence aux composés organiques et inorganiques contenant le groupe cyano.
CONTENU
1. Aperçu et différence clé
2. Qu'est-ce que le cyanure
3. Qu'est-ce que Nitrile
4. Comparaison côte à côte - Cyanure vs nitrile sous forme tabulaire
5. Résumé
Qu'est-ce que le cyanure?
Le cyanure est tout composé chimique ayant le groupe cyano (C≡N). Le groupe Cyano a un atome de carbone et un atome d'azote, qui sont liés par une triple liaison. Ainsi, le terme cyanure peut se référer à tout composé organique ou inorganique contenant le groupe cyano. En revanche, le terme nitrile fait référence à tout composé organique ayant un groupe Cyano.
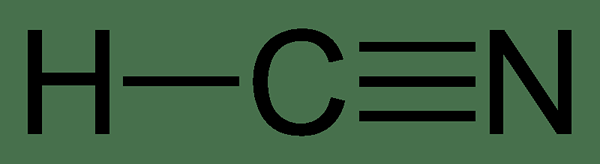
Figure 01: Structure du cyanure d'hydrogène
Habituellement, dans les cyanures inorganiques, le groupe Cyano est présent comme un anion; Par exemple, le cyanure de sodium et le cyanure de potassium. De plus, ces cyanures sont très toxiques. Le cyanure d'hydrogène ou le HCN est une substance très volatile et très toxique. Dans Nitriles, le groupe Cyano est attaché avec une liaison covalente au reste de la molécule (pas comme ion). Un exemple courant serait l'acétonitrile.
De plus, les cyanures sont produits par de nombreuses espèces de bactéries, de champignons et d'algues. C'est aussi un composant commun dans de nombreuses plantes. De plus, ces composés se forment comme un sous-produit de la combustion, dans un environnement déficiente en oxygène.
Lorsque vous envisagez les applications des cyanures, ces composés sont utiles pour l'exploitation de l'argent et de l'or car les cyanures aident à dissoudre ces métaux. De plus, les cyanures sont importants comme précurseurs pour les processus de synthèse organique, E.g., production de nylon. En outre, il existe des applications de cyanure dans le domaine de la médecine et de la lutte antiparasitaire.
Qu'est-ce que Nitrile?
Un nitrile est tout composé organique ayant un groupe -cn, et une triple liaison entre un atome de carbone et un atome d'azote. La structure moléculaire d'un nitrile est donnée comme R-C≡N. De plus, l'angle de liaison de la liaison R-C-N est de 180o. Ainsi, les groupes fonctionnels de nitriles sont des structures linéaires.
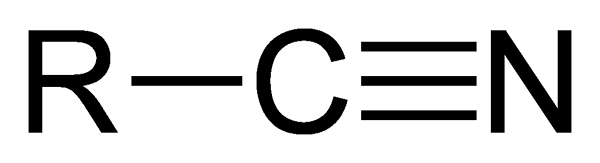
Figure 02: Structure chimique d'un composé de nitrile général
L'atome d'azote en nitrile est hautement électronégatif. En raison de la différence dans les valeurs d'électronégativité du carbone et de l'azote, une polarité est induite, faisant des composés nitriles polaires. Comme ce sont des molécules polaires, les nitriles ont des points d'ébullition plus élevés par rapport à d'autres molécules de même taille. De plus, les composés nitriles ne peuvent pas former des liaisons hydrogène (s'il n'y a pas d'autres groupes fonctionnels de formation de liaisons hydrogène). Les petits composés de nitrile sont solubles dans l'eau en raison de leur polarité, mais les grands composés en nitrile ne sont pas solubles.
Le caoutchouc de nitrile, qui est un polymère synthétique, est un exemple courant d'un nitrile important industriellement. Les monomères utilisés pour la production sont l'acrylonitrile et le butadiène. Les produits tels que les gants en caoutchouc en nitrile présentent de nombreux avantages par rapport aux produits en caoutchouc naturel. De tels exemples incluent une résistance chimique, une longue durée de conservation, une bonne résistance à la perforation, etc.
Quelle est la différence entre le cyanure et le nitrile?
Nous utilisons généralement les termes cyanure et nitrile interchangeables parce que ces deux termes se réfèrent au groupe C≡N ou au groupe Cyano. Néanmoins, la principale différence entre le cyanure et le nitrile est que le terme cyanure fait référence à tout composé chimique contenant le groupe Cyano, tandis que le terme nitrile se réfère à tout composé organique contenant le groupe cyano.
De plus, une autre différence entre le cyanure et le nitrile est que si les composés inorganiques ont un groupe Cyano comme anion, les composés organiques ont une liaison covalente entre la molécule et le groupe Cyano.
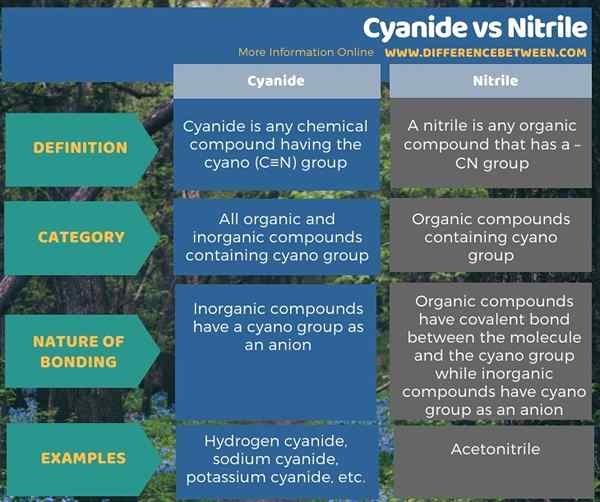
Résumé - Cyanure vs nitrile
Les termes cyanure et nitrile sont souvent utilisés de manière interchangeable car ces deux termes se réfèrent au groupe C≡N ou au groupe Cyano. La principale différence entre le cyanure et le nitrile est que le terme cyanure fait référence à tout composé chimique contenant le groupe Cyano, tandis que le terme nitrile se réfère à tout composé organique contenant le groupe cyano.
Référence:
1. "Cyanure." Wikipédia, Fondation Wikimedia, 17 septembre. 2019, disponible ici.
Image gracieuseté:
1. «Hydrogène-cyanide-2d» par hyanyd-cyanure.PNG: Ericvsesvg-Version: N-Regen - Hydrogène-cyanure.PNG (domaine public) via Commons Wikimedia
2. «Nitrile-Groupe-2d» (domaine public) via Commons Wikimedia


